6月28日,CDE官網顯示,禮來每日1次口服小分子GLP-1R激動劑LY3502970膠囊(Orforglipron)的臨牀試驗申請獲默示許可,用於減重。  LY3502970膠囊是一款新型、高效、口服的非肽類GLP-1R激動劑,最初由Chugai开發。2018年9月,禮來與Chugai達成協議,獲得LY3502970的全球开發和商業化權益。 6月23日,禮來公布了Orforglipron用於不伴有2型糖尿病的肥胖患者(平均基线體重爲109kg)的II期臨試驗具體數據,該研究已發表在《新英格蘭醫學雜志》上。 結果顯示,第26周時,Orforglipron不同劑量組(12mg, 24mg, 36mg或45mg)均具有統計學意義的劑量依賴性體重減輕,減重範圍爲8.6%(9.0kg)至12.6%(13.3kg),而安慰劑組爲2.0%(2.1kg),達到了主要終點。 到第36周時,所有劑量組患者的體重也都在持續下降,範圍在9.4%(9.8kg)至14.7%(15.4kg),而安慰劑組該數值爲2.3%(2.4kg)。
LY3502970膠囊是一款新型、高效、口服的非肽類GLP-1R激動劑,最初由Chugai开發。2018年9月,禮來與Chugai達成協議,獲得LY3502970的全球开發和商業化權益。 6月23日,禮來公布了Orforglipron用於不伴有2型糖尿病的肥胖患者(平均基线體重爲109kg)的II期臨試驗具體數據,該研究已發表在《新英格蘭醫學雜志》上。 結果顯示,第26周時,Orforglipron不同劑量組(12mg, 24mg, 36mg或45mg)均具有統計學意義的劑量依賴性體重減輕,減重範圍爲8.6%(9.0kg)至12.6%(13.3kg),而安慰劑組爲2.0%(2.1kg),達到了主要終點。 到第36周時,所有劑量組患者的體重也都在持續下降,範圍在9.4%(9.8kg)至14.7%(15.4kg),而安慰劑組該數值爲2.3%(2.4kg)。
 LY3502970膠囊是一款新型、高效、口服的非肽類GLP-1R激動劑,最初由Chugai开發。2018年9月,禮來與Chugai達成協議,獲得LY3502970的全球开發和商業化權益。 6月23日,禮來公布了Orforglipron用於不伴有2型糖尿病的肥胖患者(平均基线體重爲109kg)的II期臨試驗具體數據,該研究已發表在《新英格蘭醫學雜志》上。 結果顯示,第26周時,Orforglipron不同劑量組(12mg, 24mg, 36mg或45mg)均具有統計學意義的劑量依賴性體重減輕,減重範圍爲8.6%(9.0kg)至12.6%(13.3kg),而安慰劑組爲2.0%(2.1kg),達到了主要終點。 到第36周時,所有劑量組患者的體重也都在持續下降,範圍在9.4%(9.8kg)至14.7%(15.4kg),而安慰劑組該數值爲2.3%(2.4kg)。
LY3502970膠囊是一款新型、高效、口服的非肽類GLP-1R激動劑,最初由Chugai开發。2018年9月,禮來與Chugai達成協議,獲得LY3502970的全球开發和商業化權益。 6月23日,禮來公布了Orforglipron用於不伴有2型糖尿病的肥胖患者(平均基线體重爲109kg)的II期臨試驗具體數據,該研究已發表在《新英格蘭醫學雜志》上。 結果顯示,第26周時,Orforglipron不同劑量組(12mg, 24mg, 36mg或45mg)均具有統計學意義的劑量依賴性體重減輕,減重範圍爲8.6%(9.0kg)至12.6%(13.3kg),而安慰劑組爲2.0%(2.1kg),達到了主要終點。 到第36周時,所有劑量組患者的體重也都在持續下降,範圍在9.4%(9.8kg)至14.7%(15.4kg),而安慰劑組該數值爲2.3%(2.4kg)。 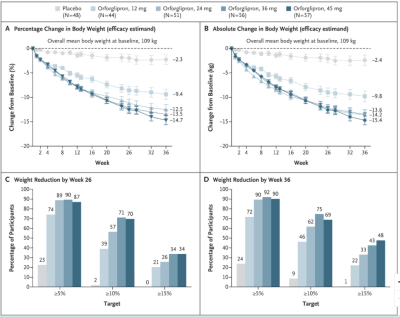
該研究也達到了所有關鍵次要終點。4個劑量組(12mg, 24mg, 36mg或45mg)體重減輕≥5%的患者比例分別爲72%、90%、92%和90%,而安慰劑組患者比例爲24%;體重減輕≥10%的患者比例分別爲47%,62%,75%和69%,而安慰劑組僅爲9%。此外,4組受試者BMI分別較基线降低3.4、4.7、5.0和5.5kg/m2(安慰劑組爲0.9kg/m2);腰圍較基线分別減少9.6、11.2, 10.6和13.6cm(安慰劑組爲4cm)。
Orforglipron的安全性與其他以腸促胰島素爲基礎的治療相似。胃腸道副作用是最常報道的不良事件,嚴重程度一般爲輕至中度,通常發生在劑量遞增期間。
目前,禮來針對Orforglipron已啓動3項III期臨牀研究,包括:對比甘精胰島素(個性化劑量,每日1次)用於心血管風險增加的肥胖或超重的2型糖尿病患者(NCT05803421),對比安慰劑治療伴有體重相關合並症的成人肥胖或超重患者(NCT05869903)以及對比安慰劑治療伴有2型糖尿病的肥胖或超重成人患者(NCT05872620)。
追加內容
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:禮來口服小分子GLP-1R激動劑減肥適應症國內首次獲批臨牀
地址:https://www.twetclubs.com/post/11387.html