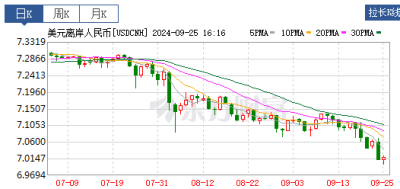
近日,Argenx公布了Vyvgart Hytrulo (efgartigimod alfa and hyaluronidase-qvfc)用於治療慢性炎性脫髓鞘性多發性神經根神經病(CIDP)成人患者的ADHERE研究的初步結果。結果顯示該研究達到了主要終點(p=0.000039)與安慰劑相比Vyvgart Hytrulo可顯著降低CIDP復發風險,ADHERE研究詳細的數據將會在即將召开的醫學會議上公布。
受利好消息影響,本周Argenx股價暴漲超過40%,截止19日收盤,市值294億美元。要知道2022年Argenx的營收只有約4.5億美元,還虧損了7億美元,那么Argenx究竟是家什么公司,有着怎樣的魔力支撐着接近300億元的市值?
一款產品撐起300億美元的市值
Argenx是一家生物科技公司,創立於2008年,總部位於荷蘭Breda,專注於开發治療自免疾病和癌症的抗體療法,擁有SIMPLE Antibody平台、NHance、ABEDEG和POTELLIGENT三項與抗體Fc區改造相關的專利技術,是技術平台類型公司。
Argenx的名字來自古希臘神話中的Argonauts英雄,這是有記錄以來最早認識到團隊力量的故事之一。Argenx希望可以通過協作的力量來更好解決免疫學治療領域的挑战。該公司2017年在納斯達克上市,當時的發行價只有17美元,近6年股價上漲近30倍。其第一款產品在2021年獲批,在此之前Argenx依靠自主开發的平台與MNC合作、授權,成爲公司融資以外的主要收入來源,這與再生元、吉利德等biopharma剛上市時的情況十分類似,其公司的發展史也是VYVGART的研發史,VYVGART研發的每一次突破都帶動公司股價上漲。
截至目前,Argenx僅一款產品上市,包括兩種劑型:VYVGART(靜脈注射)和VYVGART Hytrulo(皮下注射)。
VYVGART
2021年12月17日,FDA批准Argenx公司研發的first-in-class療法VYVGART上市,這是FDA批准的第一個用於治療乙酰膽鹼受體(AChR)抗體陽性的全身型重症肌無力(gMG)成人患者的Fc受體(FcRn)拮抗劑。
VYVGART是免疫球蛋白G(IgG)抗體的片段,靶向FcRn,旨在與新生兒FcRn結合,阻止FcRn將IgG再循環回血液中,這樣可以使IgG抗體更快耗竭,從而減輕疾病症狀。
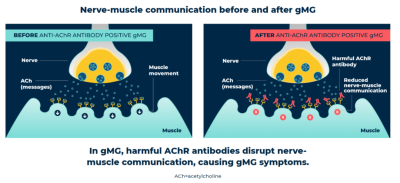
圖1 gMG前後的神經肌肉通訊,來源:Argenx官網
根據臨牀試驗結果顯示,經VYVGART治療的65人中44人(68%)日常活動能力顯著提高,安慰劑組僅有30%(19/64人);在減少肌肉無力表現上也好於安慰劑組,VYVGART組爲63%(14/65),安慰劑組爲14%(9/64)。在安全性方面至少5%接受VYVGART治療的患者出現呼吸道感染、頭痛、尿路感染、刺痛感、肌肉疼痛,與安慰劑相比出現的頻率更高。
VYVGART Hytrulo
今年6月20日,FDA批准了VYVGART Hytrulo用於治療gMG,這是FDA批准的首款gMG皮下制劑。
VYVGART Hytrulo是一種皮下產品組合,由efgartigimod alfa和重組人透明質酸酶PH20(rHuPH20)組成,rHuPH20是Halozyme的ENHANZE藥物遞送技術,可促進生物制劑的皮下遞送。VYVGART Hytrulo雖然也需要每周注射一次,持續四周,不同於靜脈注射每次需要1小時,皮下注射僅需要30-90s,大大節約了患者用藥時間。
VYVGART Hytrulo的獲批是基於全球3期ADAPT-SC研究的陽性結果,結果顯示在成年gMG患者中,與靜脈輸注相比,皮下注射劑型在第29天時總IgG的降低具有非劣效性。在第29天,與基线水平相比,皮下注射劑型平均總IgG減少66.4%,而靜脈輸注劑型爲62.2%。在安全性方面與靜脈輸注研究一致。
2021年再鼎醫藥和Argenx達成合作,再鼎醫藥將負責推進efgartigimod在大中華區(包括中國內地、香港、台灣和澳門地區)的开發和商業化工作。今年7月10再鼎醫藥宣布艾加莫德注射液(皮下注射)經NMPA獲批上市用於治療gMG。另外艾加莫德gMG適應症已經在日本、歐洲等地區上市。

圖2 艾加莫德gMG適應症全球獲批情況,來源:Argenx官網
差異化的臨牀开發更顯智慧
我們再回到文章开始的新聞,此次Argenx股價大漲的催化劑是VYVGART Hytrulo用於治療CIPD患者的ADHERE研究陽性數據。結果顯示ADHERE研究達到主要終點,與安慰劑相比,VYVGART Hytrulo可降低復發風險61% (HR: 0.39 95% CI: 0.25; 0.61);在开放標籤A階段,67%的患者確認出現臨牀改善(ECI);安全性與先前研究一致;91%(226/249)的符合條件患者繼續參加ADHERE-Plus开放標籤擴展研究。
Efgartigimod的臨牀研究不僅限於gMG和CIPD。
根據Argenx官網顯示Efgartigimod共計有15項研究13項適應症進行着臨牀研究,這13項適應症分別是gMG、原發性免疫性血小板減少症 (ITP)、尋常型天皰瘡和落葉型天皰瘡(PV和PF)、慢性炎症性脫髓鞘性多發性神經病(CIDP)、大皰性類天皰瘡(BP)、特發性炎症性肌病、新冠肺炎後體位性心動過速綜合徵(PC-POTS)、原發性幹燥綜合徵(pSS)、膜性腎病(MN)、狼瘡性腎炎(LN)、甲狀腺眼病(TED)、抗體介導的排斥反應(AMR)、ANCA相關性血管炎(AAV)。
Efgartigimod適應症的數量堪比K藥(帕博利珠單抗),這些適應症多爲罕見病,可以看出Argenx發展策略優先選擇相對藍海、未被滿足,患者相對較少的罕見病且疾病機制清晰的方向。
另外FDA對孤兒藥的研發十分鼓勵,藥物獲得FDA孤兒藥認定後有很多益處:(1)藥物獲批上市後享有7年市場獨佔權(2)免除NDA/BLA申請費用(3)臨牀研究費用享受25%稅收減免(4)可能免除或者減少臨牀數據的申報要求。這樣的开發策略一方面可以避免與大藥企正面競爭,減少公司研發壓力不用急於搶時間和研發費用,還可以贏得監管支持,提高了研發成功的概率。
自研管线中Efgartigimod之外,Argenx還在免疫驗證領域還在开發兩款FIC差異化品種,ARGX-117(多竈性運動神經病 (MMN)、移植物功能延遲恢復、皮肌炎 (DM))和ARGX-119(神經肌肉相關),另外還有一款候選藥物ARGX-118處於臨牀前。
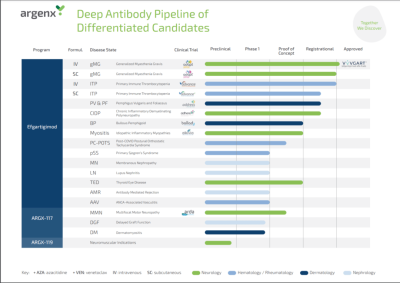
圖3 Argenx在研管线情況,來源:Argenx官網
除了自研管线,還有3款項目已經授權給其他公司進行進一步开發,分別是靶向IL22的ARGX-112(LEO Pharma正在評估用於特應性皮炎)、靶向MET的ARGX-114(具有使纖維化、炎症、自身免疫和退行性疾病患者受損組織再生的潛力)以及靶向GARP的ARGX-115((AbbVie正在研究其用於治療癌症的效果)。
重磅炸彈酝釀中
Argenx有望成爲下一個biopharma
gMG作爲一種罕見的慢性自身免疫性疾病,IgG自身抗體會破壞神經和肌肉之間的通訊,導致肌肉無力,甚至可能危及生命。大約85%的MG患者會在24個月內發展爲gMG。全球至少有70萬gMG患者,已確診具有AChR抗體的患者約佔gMG總人群的85%,gMG治療領域存在巨大的未滿足需求。
VYVGART 2022年的銷售額超4億美元,今年一季度的銷售額已經達到2.18億美元,環比增長26%,gMG領域競爭對手少隨着皮下注射以及在全球範圍獲批可以預見VYVGART放量速度將非常快,2023年銷售額翻倍不難。後續適應症如果陸續獲批,efgartigimod市場潛力巨大,Evaluate Vantage預測,2026年efgartigimod的全球銷售額將達到25億美元。
總之,如果對安進、吉利德、渤健還有再生元四家頭部Biopharma的發展史進行回望,我們不難發現從biotech公司成立到第一款產品上市一般需要10年左右,有的更長,再生元在公司成立20年之後才迎來首款上市產品列洛西普。Argenx 近300億美元的市值說明市場看好Argenx公司的發展潛力,Argenx也正一步一個腳印地向這些由biotech向Biopharma成功轉型的前輩靠近。
參考資料
1. Argenx和再鼎醫藥官網以及網上其他公开資料。
2. 德邦證券(Argenx:在免疫藍海市場孕育下一代大單品)。
來源:藥智頭條 ,作者九思
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:煜森資本:大漲40%,VYVGART能否撐起Argenx300億美元市值?
地址:https://www.twetclubs.com/post/15136.html